검색결과
-
![[특집-기술위원회] TC 215 - 의료 정보학(Health informatics)](http://www.stdnews.kr/data/file/news/thumb/thumb-32068165_7HDAVCBF_87cd4effcac1b626d770aadf6bb9d9045d64b00f_200x180.jpg) [특집-기술위원회] TC 215 - 의료 정보학(Health informatics)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.또한 △1962년 TC 105~107 △1963년 TC 108~111 △1964년 TC 112~115, TC 117 △1965년 TC 118 △1966년 TC 119~122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146~150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~161 △1975년 TC 162~164 등도 포함된다.그리고 △1976년 TC 165, TC 166 △1977년 TC 167, TC 168, TC 170 △1978년 TC 171~174 △1979년 TC 176, TC 178 △1980년 TC 180, TC 181 △1981년 TC 182 △1983년 TC 183~186 △1984년 TC 188 △1985년 TC 189~191 △1988년 TC 192~194 △1989년 TC 195 △1990년 TC 197, TC 198 △1991년 TC 199, TC 201, TC 202 △1992년 TC 204~206 △1993년 TC 209 △1994년 TC 210, TC 211 △1996년 TC 213, TC 214 등이 있다.ISO/TC 215 의료 정보학(Health informatics)과 관련된 기술위원회는 1998년 결성됐다. 사무국은 미국 표준협회(American National Standards Institute, ANSI)에서 맡고 있다.위원회는 레이첼 호손(Ms Rachel Hawthorne)가 책임지고 있다. 현재 의장은 토드 쿠퍼(Mr Todd Cooper)이며 임기는 2026년 말까지다. ISO 기술 프로그램 관리자는 마호 다카하시(Mme Maho Takahashi), ISO 편집 관리자는 발레리아 아가넨노네(Ms Valeria Agamennone) 등이다.범위는 의료 관련 데이터, 의료 시스템의 모든 측면을 지원하고 활성화하는 지식의 수집, 교환 및 사용을 촉진하기 위한 의료 정보학 분야의 표준화다.현재 ISO/TC 215 사무국과 관련해 발행된 표준은 237개며 ISO/TC 215 사무국의 직접적인 책임 하에 발행된 표준은 225개다.ISO/TC 215과 관련해 개발 중인 표준은 64개며 이중 ISO/TC 215 사무국의 직접적인 책임 하에 개발 중인 표준은 62개다. 참여하고 있는 회원은 35개국, 참관 회원은 32개국이다.□ ISO/TC 215 사무국의 직접적인 책임 하에 발행된 표준 225개 중 15개 목록▷ISO 1828:2012 Health informatics — Categorial structure for terminological systems of surgical procedures▷ISO/TR 4421:2023 Health informatics — Introduction to Ayurveda informatics▷ISO/TS 5044:2023 Health informatics — Information model for quality control of traditional Chinese medicinal products▷ISO/TS 5118:2022 Health informatics — Categorial structure of representation for evaluation of clinical practice guidelines of traditional Chinese medicine▷ISO/TS 5346:2022 Health informatics — Categorial structure for representation of traditional Chinese medicine clinical decision support system▷ISO 5477:2023 Health informatics — Interoperability of public health emergency preparedness and response information systems▷ISO/TS 5499:2024 Health informatics — Clinical particulars — Core principles for the harmonization of therapeutic indications terms and identifiers▷ISO/TS 5568:2022 Health informatics — Traditional Chinese medicine — Labelling metadata of human biological sample information▷ISO/TS 5569:2023 Health informatics — Conceptual data model for Chinese medicinal herbs▷ISO/TR 9143:2023 Health informatics — Sex and gender in electronic health records▷ISO 10159:2011 Health informatics — Messages and communication — Web access reference manifest▷ISO 10781:2023 Health informatics — HL7 Electronic Health Record-System Functional Model, Release 2.1 (EHR FM)▷ISO/IEEE 11073-00103:2015 Health informatics — Personal health device communication — Part 00103: Overview▷ISO/IEEE 11073-10101:2020 Health informatics — Device interoperability — Part 10101: Point-of-care medical device communication — Nomenclature▷ISO/IEEE 11073-10102:2014 Health informatics — Point-of-care medical device communication — Part 10102: Nomenclature — Annotated ECG□ ISO/TC 215 사무국의 직접적인 책임 하에 개발 중인 표준 62개 중 15개 목록▷ISO/AWI TR 4419 Health informatics — Reducing clinicians burden▷ISO/DTS 5384 Health informatics - Categorial Structure and Data Elements for the Identification and Exchange of Immunization Data▷ISO/CD TS 5615 Health informatics — Accelerating Safe, Effective and Secure Remote Connected Care and Mobile Health Through Standards-Based Interoperability Solutions Addressing Gaps Revealed by Pandemics▷ISO/DTS 5777 Health informatics — The architecture of internet healthcare service network▷ISO/DTS 5788 Health informatics — Internet healthcare service pattern▷ISO/CD TS 6201.2 Health Informatics — Personalized Digital Health -Framework▷ISO/CD TS 6204 Health Informatics — Categorial structures for representation of Ayurvedic medicinal water — Decocting process in Ayurveda▷ISO/AWI TS 6226 Health informatics — Reference architecture for syndromic surveillance systems for infectious diseases▷ISO/DTR 6231 Health informatics — Standardizing graphical content▷ISO/CD TS 6268-1 Health informatics — Cybersecurity framework for telehealth environments — Part 1: Overview and Concepts▷ISO/AWI TS 6268-2 Health informatics — Cybersecurity framework for telehealth environments — Part 2: Cybersecurity reference models of telehealth▷ISO/CD TS 7122 Health Informatics — Guidelines for exchanging data generated by POCT (Point of Care Testing) devices between screening center and clinical laboratory▷ISO/AWI TS 9166 Health Informatics — Guidelines for self-assessment questionnaire systems▷ISO/DTS 9320 Health informatics — Standardized data set for transfer of hemodialysis patients▷ISO/DTS 9321 Health informatics — General requirements of multi-centre medical data collaborative analysis□ ISO/TC 215 사무국 분과위원회(Subcommittee)의 책임 하에 발행 및 개발 중인 표준 현황▷ISO/TC 215/SC 1 Genomics Informatics ; 발행된 표준 12개, 개발 중인 표준 2개
[특집-기술위원회] TC 215 - 의료 정보학(Health informatics)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.또한 △1962년 TC 105~107 △1963년 TC 108~111 △1964년 TC 112~115, TC 117 △1965년 TC 118 △1966년 TC 119~122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146~150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~161 △1975년 TC 162~164 등도 포함된다.그리고 △1976년 TC 165, TC 166 △1977년 TC 167, TC 168, TC 170 △1978년 TC 171~174 △1979년 TC 176, TC 178 △1980년 TC 180, TC 181 △1981년 TC 182 △1983년 TC 183~186 △1984년 TC 188 △1985년 TC 189~191 △1988년 TC 192~194 △1989년 TC 195 △1990년 TC 197, TC 198 △1991년 TC 199, TC 201, TC 202 △1992년 TC 204~206 △1993년 TC 209 △1994년 TC 210, TC 211 △1996년 TC 213, TC 214 등이 있다.ISO/TC 215 의료 정보학(Health informatics)과 관련된 기술위원회는 1998년 결성됐다. 사무국은 미국 표준협회(American National Standards Institute, ANSI)에서 맡고 있다.위원회는 레이첼 호손(Ms Rachel Hawthorne)가 책임지고 있다. 현재 의장은 토드 쿠퍼(Mr Todd Cooper)이며 임기는 2026년 말까지다. ISO 기술 프로그램 관리자는 마호 다카하시(Mme Maho Takahashi), ISO 편집 관리자는 발레리아 아가넨노네(Ms Valeria Agamennone) 등이다.범위는 의료 관련 데이터, 의료 시스템의 모든 측면을 지원하고 활성화하는 지식의 수집, 교환 및 사용을 촉진하기 위한 의료 정보학 분야의 표준화다.현재 ISO/TC 215 사무국과 관련해 발행된 표준은 237개며 ISO/TC 215 사무국의 직접적인 책임 하에 발행된 표준은 225개다.ISO/TC 215과 관련해 개발 중인 표준은 64개며 이중 ISO/TC 215 사무국의 직접적인 책임 하에 개발 중인 표준은 62개다. 참여하고 있는 회원은 35개국, 참관 회원은 32개국이다.□ ISO/TC 215 사무국의 직접적인 책임 하에 발행된 표준 225개 중 15개 목록▷ISO 1828:2012 Health informatics — Categorial structure for terminological systems of surgical procedures▷ISO/TR 4421:2023 Health informatics — Introduction to Ayurveda informatics▷ISO/TS 5044:2023 Health informatics — Information model for quality control of traditional Chinese medicinal products▷ISO/TS 5118:2022 Health informatics — Categorial structure of representation for evaluation of clinical practice guidelines of traditional Chinese medicine▷ISO/TS 5346:2022 Health informatics — Categorial structure for representation of traditional Chinese medicine clinical decision support system▷ISO 5477:2023 Health informatics — Interoperability of public health emergency preparedness and response information systems▷ISO/TS 5499:2024 Health informatics — Clinical particulars — Core principles for the harmonization of therapeutic indications terms and identifiers▷ISO/TS 5568:2022 Health informatics — Traditional Chinese medicine — Labelling metadata of human biological sample information▷ISO/TS 5569:2023 Health informatics — Conceptual data model for Chinese medicinal herbs▷ISO/TR 9143:2023 Health informatics — Sex and gender in electronic health records▷ISO 10159:2011 Health informatics — Messages and communication — Web access reference manifest▷ISO 10781:2023 Health informatics — HL7 Electronic Health Record-System Functional Model, Release 2.1 (EHR FM)▷ISO/IEEE 11073-00103:2015 Health informatics — Personal health device communication — Part 00103: Overview▷ISO/IEEE 11073-10101:2020 Health informatics — Device interoperability — Part 10101: Point-of-care medical device communication — Nomenclature▷ISO/IEEE 11073-10102:2014 Health informatics — Point-of-care medical device communication — Part 10102: Nomenclature — Annotated ECG□ ISO/TC 215 사무국의 직접적인 책임 하에 개발 중인 표준 62개 중 15개 목록▷ISO/AWI TR 4419 Health informatics — Reducing clinicians burden▷ISO/DTS 5384 Health informatics - Categorial Structure and Data Elements for the Identification and Exchange of Immunization Data▷ISO/CD TS 5615 Health informatics — Accelerating Safe, Effective and Secure Remote Connected Care and Mobile Health Through Standards-Based Interoperability Solutions Addressing Gaps Revealed by Pandemics▷ISO/DTS 5777 Health informatics — The architecture of internet healthcare service network▷ISO/DTS 5788 Health informatics — Internet healthcare service pattern▷ISO/CD TS 6201.2 Health Informatics — Personalized Digital Health -Framework▷ISO/CD TS 6204 Health Informatics — Categorial structures for representation of Ayurvedic medicinal water — Decocting process in Ayurveda▷ISO/AWI TS 6226 Health informatics — Reference architecture for syndromic surveillance systems for infectious diseases▷ISO/DTR 6231 Health informatics — Standardizing graphical content▷ISO/CD TS 6268-1 Health informatics — Cybersecurity framework for telehealth environments — Part 1: Overview and Concepts▷ISO/AWI TS 6268-2 Health informatics — Cybersecurity framework for telehealth environments — Part 2: Cybersecurity reference models of telehealth▷ISO/CD TS 7122 Health Informatics — Guidelines for exchanging data generated by POCT (Point of Care Testing) devices between screening center and clinical laboratory▷ISO/AWI TS 9166 Health Informatics — Guidelines for self-assessment questionnaire systems▷ISO/DTS 9320 Health informatics — Standardized data set for transfer of hemodialysis patients▷ISO/DTS 9321 Health informatics — General requirements of multi-centre medical data collaborative analysis□ ISO/TC 215 사무국 분과위원회(Subcommittee)의 책임 하에 발행 및 개발 중인 표준 현황▷ISO/TC 215/SC 1 Genomics Informatics ; 발행된 표준 12개, 개발 중인 표준 2개 -
 식약처, 제24차 국제의료기기규제당국자포럼 정기총회 참석정부가 제24차 국제의료기기규제당국자포럼(IMDRF) 정기총회에 참석해 국가별 디지털헬스 규제 현황을 논의하고 국내 디지털의료기기 관련 제도를 홍보했다. 식품의약품안전처는 의료기기 분야 국제 규제 조화에 기여하고 디지털 헬스케어 분야 국제 규제를 선도하기 위해 독일 베를린에서 9월 25일부터 29일까지 개최된 ‘제24차 국제의료기기규제당국자포럼(IMDRF) 정기총회’에 참석했다고 밝혔다. IMDRF(International Medical Device Regulators Forum)는 의료기기 국제 규제조화를 주도하는 미국·유럽 등 11개국 규제당국자 협의체로 우리나라는 2017년 12월 가입했으며 2021년에는 1년간 의장국을 맡아 수행했다. 이번 총회에서는 ▲디지털헬스 규제현황 등 국가별 규제 현황 ▲신속심사제도 도입 ▲IMDRF-GHWP 간 협력 방안 등에 대해 논의했다. GHWP(Global Harmonization Working Party)는 아시아를 비롯 전 세계 33개 회원국이 참여하는 의료기기 규제조화를 위한 국가 간 협력기구다. 식약처는 이번 정기총회 기간 중 일본·호주 등에 우리나라의 MDSAP 참관국 전환을 위한 협조와 지지를 요청했으며 우리나라가 강점을 보이고 있는 인공지능 분야 가이드라인 공동 개발 등을 위한 국가 간 협력 강화 등을 위해 노력했다고 전했다. MDSAP(Medical Device Single Audit Program)는 미국, 일본 등 5개 정회원국으로 구성됐으며 한 번의 제조품질관리 심사로 각 국가별 심사 전부 또는 일부를 상호 인정하는 공동심사프로그램이다. MDSAP 회원은 정회원, 참관회원, 협력회원으로 구분되며 우리나라는 2019년 협력회원으로 가입해 활동 중이며 향후 참관회원을 거쳐 정회원 가입 추진 중이다. 향후 국가 간 온라인 설명회, 공동워크숍 등을 통해 국가 간 규제 제도에 대한 이해를 높이고 협력방안 등을 논의함으로써 의료기기 분야 국가 간 협력 강화를 지속적으로 추진할 예정이다. 한편 식약처는 국내 의료기기 규제체계와 제품의 우수성을 알리기 위해 국내 규제 혁신 사례, 국내 법령·가이드라인 제·개정 현황 등을 소개했다. 특히 특정 환자군을 위한 의료기기 세션에서 희소·긴급 도입 필요 의료기기 정책을, 패널 토의에서 디지털 치료기기 특성과 관련 규제를 발표해 국내 의료기기 분야 규제 우수성을 널리 알렸다. 또한 이번 총회에 국내 의료기기 산업계를 대표해 참석한 업체들은 국내 디지털치료기기에 대한 혁신의료기기 지정 제도와 자사 혁신의료기기의 임상시험 결과 등을 설명했다. 식약처 관계자는 “이번 IMDRF 정기총회가 해외 의료기기 규제기관과 협력체계를 공고히 하고 MDSAP 활동 강화 등 우리나라 규제의 영향력을 높이는 계기가 될 것으로 기대한다”고 전했다.
식약처, 제24차 국제의료기기규제당국자포럼 정기총회 참석정부가 제24차 국제의료기기규제당국자포럼(IMDRF) 정기총회에 참석해 국가별 디지털헬스 규제 현황을 논의하고 국내 디지털의료기기 관련 제도를 홍보했다. 식품의약품안전처는 의료기기 분야 국제 규제 조화에 기여하고 디지털 헬스케어 분야 국제 규제를 선도하기 위해 독일 베를린에서 9월 25일부터 29일까지 개최된 ‘제24차 국제의료기기규제당국자포럼(IMDRF) 정기총회’에 참석했다고 밝혔다. IMDRF(International Medical Device Regulators Forum)는 의료기기 국제 규제조화를 주도하는 미국·유럽 등 11개국 규제당국자 협의체로 우리나라는 2017년 12월 가입했으며 2021년에는 1년간 의장국을 맡아 수행했다. 이번 총회에서는 ▲디지털헬스 규제현황 등 국가별 규제 현황 ▲신속심사제도 도입 ▲IMDRF-GHWP 간 협력 방안 등에 대해 논의했다. GHWP(Global Harmonization Working Party)는 아시아를 비롯 전 세계 33개 회원국이 참여하는 의료기기 규제조화를 위한 국가 간 협력기구다. 식약처는 이번 정기총회 기간 중 일본·호주 등에 우리나라의 MDSAP 참관국 전환을 위한 협조와 지지를 요청했으며 우리나라가 강점을 보이고 있는 인공지능 분야 가이드라인 공동 개발 등을 위한 국가 간 협력 강화 등을 위해 노력했다고 전했다. MDSAP(Medical Device Single Audit Program)는 미국, 일본 등 5개 정회원국으로 구성됐으며 한 번의 제조품질관리 심사로 각 국가별 심사 전부 또는 일부를 상호 인정하는 공동심사프로그램이다. MDSAP 회원은 정회원, 참관회원, 협력회원으로 구분되며 우리나라는 2019년 협력회원으로 가입해 활동 중이며 향후 참관회원을 거쳐 정회원 가입 추진 중이다. 향후 국가 간 온라인 설명회, 공동워크숍 등을 통해 국가 간 규제 제도에 대한 이해를 높이고 협력방안 등을 논의함으로써 의료기기 분야 국가 간 협력 강화를 지속적으로 추진할 예정이다. 한편 식약처는 국내 의료기기 규제체계와 제품의 우수성을 알리기 위해 국내 규제 혁신 사례, 국내 법령·가이드라인 제·개정 현황 등을 소개했다. 특히 특정 환자군을 위한 의료기기 세션에서 희소·긴급 도입 필요 의료기기 정책을, 패널 토의에서 디지털 치료기기 특성과 관련 규제를 발표해 국내 의료기기 분야 규제 우수성을 널리 알렸다. 또한 이번 총회에 국내 의료기기 산업계를 대표해 참석한 업체들은 국내 디지털치료기기에 대한 혁신의료기기 지정 제도와 자사 혁신의료기기의 임상시험 결과 등을 설명했다. 식약처 관계자는 “이번 IMDRF 정기총회가 해외 의료기기 규제기관과 협력체계를 공고히 하고 MDSAP 활동 강화 등 우리나라 규제의 영향력을 높이는 계기가 될 것으로 기대한다”고 전했다. -
![[특집] ISO/TC 59 기술위원회(Technical Committees) 소개](http://www.stdnews.kr/data/file/news/thumb/thumb-3745426529_JRlrV2nd_57f4c74608b650c67dcc515027815d7c5cdf1349_200x180.jpg) [특집] ISO/TC 59 기술위원회(Technical Committees) 소개스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC1~TC323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC1 기술위원회를 시작으로 최근 순환경제를 표준화하기 위한 TC323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.ISO/TC 59 건축 및 토목공사(Buildings and civil engineering works)와 관련된 기술위원회는 TC1, TC2, TC4~TC6, TC8, TC10~TC12, TC14, TC17~TC22, TC24~31, TC33~TC39, TC41~TC48, TC51, TC52, TC54, TC58과 동일하게 1947년 구성됐다.사무국은 노르웨이표준기구(Standards Norway, SN)에서 맡고 있다. 위원회는 헤게 숄리(Ms Hege Sjølie)이 책임진다. 의장은 욘스 쇼그렌(Mr Jøns Sjøgren)으로 임기는 2027년까지다.ISO 기술 프로그램 관리자는 앤 캐서린 로(Dr Anna Caterina Rossi), ISO 편집 관리자는 이본 헨(Mrs Yvonne Chen) 등으로 조사됐다. 범위는 아래 내용을 포함하는 건축 및 토목공사 분야의 표준화다.■ 포함 내용 : ▶일반 용어▶설계, 제조 및 건설 과정에서 정보 구성▶모듈 조정 및 기본 원칙, 조인트·공차 및 맞춤에 대한 일반 규칙, 실런트에 대한 성능 및 테스트 표준 등을 포함한 건물, 건물 요소 및 구성 요소에 대한 일반적인 기하학적 요구 사항▶서비스 수명, 지속 가능성, 접근성 및 유용성과 관련된 기능 및 사용자 요구 사항을 포함한 기타 성능 요구 사항에 대한 일반 규칙▶경제적, 환경적, 사회적 영향 및 지속 가능한 개발과 관련된 측면을 다루기 위한 일반 규칙 및 지침▶별도의 ISO 기술 위원회 범위에 속하지 않는 구성 요소에 대한 형상 및 성능 요구 사항▶조달 프로세스, 방법 및 절차 등이다.■ 제외 내용 : ▶기술 제품 문서의 표준화 및 조정(ISO/TC 10)▶음향 요구 사항(ISO / TC 43)▶콘크리트 구조물 설계를 위한 기초(ISO/TC 71/SC 4)▶건축 자재, 구성 요소 및 구조와 관련된 화재 테스트 및 화재 안전 공학(ISO/TC 92)▶구조물 설계의 기초(ISO / TC 98)▶건설 기계(ISO/TC 127 및 ISO/TC 195)▶건물 유리에 대한 성능 요구 사항(ISO/TC 160)▶문, 문틀 및 창문에 대한 성능 요구 사항(ISO/TC 162)▶열적 특성 계산(ISO / TC 163)▶목재 구조물 설계를 위한 기초(ISO/TC 165)▶강철 및 알루미늄 구조의 설계 기반(ISO/TC 167)▶지질 공학 측면 및 토양 품질(ISO/TC 182 및 ISO/TC 190)▶수용 가능한 실내 환경 및 실용적인 에너지 사용에 관한 설계 및 개조 건물의 표준화(ISO/TC 205) 등이다.현재 ISO/TC 59 사무국의 직접적인 책임하에 있는 발행된 표준은 23개며 ISO/TC 59 사무국과 관련해 발행된 표준은 135개다.ISO/TC 59 사무국의 직접적인 책임하에 개발 중인 표준은 3개며 ISO/TC 59 사무국과 관련해 개발 중인 표준은 19개다. 참여하고 있는 회원은 26명, 참관 회원은 54명이다.□ ISO/TC 58 사무국의 직접 책임하에 발행된 표준 11개 목록▲ISO 3443-1:1979 Tolerances for building — Part 1: Basic principles for evaluation and specification▲ISO 3443-2:1979 Tolerances for building — Part 2: Statistical basis for predicting fit between components having a normal distribution of sizes▲ISO 3443-3:1987 Tolerances for building — Part 3: Procedures for selecting target size and predicting fit▲ISO 3443-4:1986 Tolerances for building — Part 4: Method for predicting deviations of assemblies and for allocation of tolerances▲ISO 3443-5:1982 Building construction — Tolerances for building — Part 5: Series of values to be used for specification of tolerances▲ISO 3443-6:1986 Tolerances for building — Part 6: General principles for approval criteria, control of conformity with dimensional tolerance specifications and statistical control — Method 1▲ISO 3443-7:1988 Tolerances for building — Part 7: General principles for approval criteria, control of conformity with dimensional tolerance specifications and statistical control — Method 2 (Statistical control method)▲ISO 3443-8:1989 Tolerances for building — Part 8: Dimensional inspection and control of construction work▲ISO 4463-1:1989 Measurement methods for building — Setting-out and measurement — Part 1: Planning and organization, measuring procedures, acceptance criteria▲ISO 4463-2:1995 Measurement methods for building — Setting-out and measurement — Part 2: Measuring stations and targets▲ISO 4463-3:1995 Measurement methods for building — Setting-out and measurement — Part 3: Check-lists for the procurement of surveys and measurement services▲ISO 6589:1983 Joints in building — Laboratory method of test for air permeability of joints▲ISO 7077:1981 Measuring methods for building — General principles and procedures for the verification of dimensional compliance▲ISO 7737:1986 Tolerances for building — Presentation of dimensional accuracy data▲ISO 7844:1985 Grooved vertical joints with connecting bars and concrete infill between large reinforced concrete panels — Laboratory mechanical tests — Effect of tangential loading□ ISO/TC 5 사무국의 직접 책임하에 개발 중인 표준 3개 목록▲ISO/CD 4931-1 Buildings and civil engineering works — Principles, framework and guidance for resilience design — Part 1: Adaptation to climate change▲ISO/TR 5202 Buildings and civil engineering works — Building resilience strategies related to public health emergencies — Compilation of relevant information▲ISO/AWI TR 18961 Buildings and civil engineering works – Seismic resilience assessment and strategies – Compilation of relevant information□ ISO/TC 45 사무국의 소위원회(Subcommittee)의 책임하에 발행 및 개발 중인 표준 현황▲ISO/TC 59/SC 2 Terminology and harmonization of languages ; 발행된 표준 5개, 개발 중인 표준 0개▲ISO/TC 59/SC 8 Sealants ; 발행된 표준 38개, 개발 중인 표준 2개▲ISO/TC 59/SC 13 Organization and digitization of information about buildings and civil engineering works, including building information modelling (BIM) ; 발행된 표준 21개, 개발 중인 표준 8개▲ISO/TC 59/SC 14 Design life ; 발행된 표준 10개, 개발 중인 표준 3개▲ISO/TC 59/SC 15 Framework for the description of housing performance ; 발행된 표준 5개, 개발 중인 표준 0개▲ISO/TC 59/SC 16 Accessibility and usability of the built environment ; 발행된 표준 1개, 개발 중인 표준 1개▲ISO/TC 59/SC 17 Sustainability in buildings and civil engineering works ; 발행된 표준 13개, 개발 중인 표준 1개▲ISO/TC 59/SC 18 Construction procurement ; 발행된 표준 9개, 개발 중인 표준 1개▲ISO/TC 59/SC 19 Prefabricated building ; 발행된 표준 10개, 개발 중인 표준 0개
[특집] ISO/TC 59 기술위원회(Technical Committees) 소개스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC1~TC323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC1 기술위원회를 시작으로 최근 순환경제를 표준화하기 위한 TC323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.ISO/TC 59 건축 및 토목공사(Buildings and civil engineering works)와 관련된 기술위원회는 TC1, TC2, TC4~TC6, TC8, TC10~TC12, TC14, TC17~TC22, TC24~31, TC33~TC39, TC41~TC48, TC51, TC52, TC54, TC58과 동일하게 1947년 구성됐다.사무국은 노르웨이표준기구(Standards Norway, SN)에서 맡고 있다. 위원회는 헤게 숄리(Ms Hege Sjølie)이 책임진다. 의장은 욘스 쇼그렌(Mr Jøns Sjøgren)으로 임기는 2027년까지다.ISO 기술 프로그램 관리자는 앤 캐서린 로(Dr Anna Caterina Rossi), ISO 편집 관리자는 이본 헨(Mrs Yvonne Chen) 등으로 조사됐다. 범위는 아래 내용을 포함하는 건축 및 토목공사 분야의 표준화다.■ 포함 내용 : ▶일반 용어▶설계, 제조 및 건설 과정에서 정보 구성▶모듈 조정 및 기본 원칙, 조인트·공차 및 맞춤에 대한 일반 규칙, 실런트에 대한 성능 및 테스트 표준 등을 포함한 건물, 건물 요소 및 구성 요소에 대한 일반적인 기하학적 요구 사항▶서비스 수명, 지속 가능성, 접근성 및 유용성과 관련된 기능 및 사용자 요구 사항을 포함한 기타 성능 요구 사항에 대한 일반 규칙▶경제적, 환경적, 사회적 영향 및 지속 가능한 개발과 관련된 측면을 다루기 위한 일반 규칙 및 지침▶별도의 ISO 기술 위원회 범위에 속하지 않는 구성 요소에 대한 형상 및 성능 요구 사항▶조달 프로세스, 방법 및 절차 등이다.■ 제외 내용 : ▶기술 제품 문서의 표준화 및 조정(ISO/TC 10)▶음향 요구 사항(ISO / TC 43)▶콘크리트 구조물 설계를 위한 기초(ISO/TC 71/SC 4)▶건축 자재, 구성 요소 및 구조와 관련된 화재 테스트 및 화재 안전 공학(ISO/TC 92)▶구조물 설계의 기초(ISO / TC 98)▶건설 기계(ISO/TC 127 및 ISO/TC 195)▶건물 유리에 대한 성능 요구 사항(ISO/TC 160)▶문, 문틀 및 창문에 대한 성능 요구 사항(ISO/TC 162)▶열적 특성 계산(ISO / TC 163)▶목재 구조물 설계를 위한 기초(ISO/TC 165)▶강철 및 알루미늄 구조의 설계 기반(ISO/TC 167)▶지질 공학 측면 및 토양 품질(ISO/TC 182 및 ISO/TC 190)▶수용 가능한 실내 환경 및 실용적인 에너지 사용에 관한 설계 및 개조 건물의 표준화(ISO/TC 205) 등이다.현재 ISO/TC 59 사무국의 직접적인 책임하에 있는 발행된 표준은 23개며 ISO/TC 59 사무국과 관련해 발행된 표준은 135개다.ISO/TC 59 사무국의 직접적인 책임하에 개발 중인 표준은 3개며 ISO/TC 59 사무국과 관련해 개발 중인 표준은 19개다. 참여하고 있는 회원은 26명, 참관 회원은 54명이다.□ ISO/TC 58 사무국의 직접 책임하에 발행된 표준 11개 목록▲ISO 3443-1:1979 Tolerances for building — Part 1: Basic principles for evaluation and specification▲ISO 3443-2:1979 Tolerances for building — Part 2: Statistical basis for predicting fit between components having a normal distribution of sizes▲ISO 3443-3:1987 Tolerances for building — Part 3: Procedures for selecting target size and predicting fit▲ISO 3443-4:1986 Tolerances for building — Part 4: Method for predicting deviations of assemblies and for allocation of tolerances▲ISO 3443-5:1982 Building construction — Tolerances for building — Part 5: Series of values to be used for specification of tolerances▲ISO 3443-6:1986 Tolerances for building — Part 6: General principles for approval criteria, control of conformity with dimensional tolerance specifications and statistical control — Method 1▲ISO 3443-7:1988 Tolerances for building — Part 7: General principles for approval criteria, control of conformity with dimensional tolerance specifications and statistical control — Method 2 (Statistical control method)▲ISO 3443-8:1989 Tolerances for building — Part 8: Dimensional inspection and control of construction work▲ISO 4463-1:1989 Measurement methods for building — Setting-out and measurement — Part 1: Planning and organization, measuring procedures, acceptance criteria▲ISO 4463-2:1995 Measurement methods for building — Setting-out and measurement — Part 2: Measuring stations and targets▲ISO 4463-3:1995 Measurement methods for building — Setting-out and measurement — Part 3: Check-lists for the procurement of surveys and measurement services▲ISO 6589:1983 Joints in building — Laboratory method of test for air permeability of joints▲ISO 7077:1981 Measuring methods for building — General principles and procedures for the verification of dimensional compliance▲ISO 7737:1986 Tolerances for building — Presentation of dimensional accuracy data▲ISO 7844:1985 Grooved vertical joints with connecting bars and concrete infill between large reinforced concrete panels — Laboratory mechanical tests — Effect of tangential loading□ ISO/TC 5 사무국의 직접 책임하에 개발 중인 표준 3개 목록▲ISO/CD 4931-1 Buildings and civil engineering works — Principles, framework and guidance for resilience design — Part 1: Adaptation to climate change▲ISO/TR 5202 Buildings and civil engineering works — Building resilience strategies related to public health emergencies — Compilation of relevant information▲ISO/AWI TR 18961 Buildings and civil engineering works – Seismic resilience assessment and strategies – Compilation of relevant information□ ISO/TC 45 사무국의 소위원회(Subcommittee)의 책임하에 발행 및 개발 중인 표준 현황▲ISO/TC 59/SC 2 Terminology and harmonization of languages ; 발행된 표준 5개, 개발 중인 표준 0개▲ISO/TC 59/SC 8 Sealants ; 발행된 표준 38개, 개발 중인 표준 2개▲ISO/TC 59/SC 13 Organization and digitization of information about buildings and civil engineering works, including building information modelling (BIM) ; 발행된 표준 21개, 개발 중인 표준 8개▲ISO/TC 59/SC 14 Design life ; 발행된 표준 10개, 개발 중인 표준 3개▲ISO/TC 59/SC 15 Framework for the description of housing performance ; 발행된 표준 5개, 개발 중인 표준 0개▲ISO/TC 59/SC 16 Accessibility and usability of the built environment ; 발행된 표준 1개, 개발 중인 표준 1개▲ISO/TC 59/SC 17 Sustainability in buildings and civil engineering works ; 발행된 표준 13개, 개발 중인 표준 1개▲ISO/TC 59/SC 18 Construction procurement ; 발행된 표준 9개, 개발 중인 표준 1개▲ISO/TC 59/SC 19 Prefabricated building ; 발행된 표준 10개, 개발 중인 표준 0개 -
 식약처, 국제 리더쉽으로 규제장벽 넘어 의료기기 수출 지원한다식품의약품안전처(처장 오유경)는 2월 13일부터 16일까지 국제의료기기규제조화회의(GHWP*, 사우디아라비아 리아드) 연례총회에 참석하여 디지털헬스 글로벌 중심국가로 도약하기 위한 의료기기 분야 국제 협력 네트워크를 강화하고 국산 제품의 수출지원 방안을 모색했다. * GHWP(Global Harmonization Working Party) : 의료기기 국제 규제 조화를 위해 1996년 발족한 협력기구. 현재 미국, 일본, 중국, 싱가포르 등 세계 33개 회원국에서 참여 중이며, 기술위원회(Technical Committee)와 9개의 실무그룹(Working Group)으로 구성. 우리나라는 ’15~’17년 의장국 수행 이번 총회에서 식약처는 우수한 허가·심사 규제역량을 인정받아 ‘의료기기 허가 실무그룹(실무그룹1)’ 의장직을 연임(3년 임기)하게 되었다. 아울러 식약처는 IMDRF* 의장국으로 활동하면서 식약처의 인공지능 의료기기 가이드라인을 국제 공통 가이드라인으로 채택시킨 경험과 전문성을 바탕으로, GHWP에서 식약처의 ‘인공지능 기반 조직병리 체외진단 의료기기(소프트웨어) 허가심사 가이드라인’을 국제 공통 가이드라인으로 채택하기 위한 논의를 시작했다. * 국제의료기기규제당국자포럼(International Medical Device Regulatory Forum, IMDRF) : 의료기기 사전·사후 전주기에 대한 국제 규제 조화·단일화를 촉진하기 위해 구성된 미국 유럽 등 11개국 규제당국자 간 협의체. 우리나라는 ’21년 의장국으로 활동 또한 이번 총회에서는 GHWP 회원국이 의료기기의 허가사항을 변경할 때 적용하는 가이드라인*에 식약처의 ‘인공지능 의료기기 허가심사 가이드라인’이 중요한 참고 가이드라인으로 추가되었다. * Categorization of Changes to a Registered Medical Device 참고로 이번 GHWP 연례총회에서 ‘디지털헬스기기의 적용 확대’를 특별 주제로 선정해 논의했으며, 우리나라는 식약처, 산업계, 병원 등에서 연자로 참석하여 국내 선진 규제 시스템과 혁신제품 활용사례를 발표했다. 특히 선제적 가이드라인 마련 등 맞춤형 규제지원을 받아 국내 최초로 허가된 디지털치료기기*, 디지털 기술이 적용된 스마트병원, 다양한 인공지능 의료기기 활용사례 등이 많은 관심을 받았다. * 불면증 인지행동 치료용 디지털치료기기(’23.2.15. 허가) 식약처는 앞으로 규제과학 전문성을 기반으로 GPS* 전략을 적극 추진하여 의료기기 분야 국제 규제 조화를 선도하고 우수한 국산 의료기기의 해외시장 진출을 지원하겠다고 밝혔다. * G(글로벌 리더로 도약), P(국제 파트너쉽 확대), S(수출지원 서포터)
식약처, 국제 리더쉽으로 규제장벽 넘어 의료기기 수출 지원한다식품의약품안전처(처장 오유경)는 2월 13일부터 16일까지 국제의료기기규제조화회의(GHWP*, 사우디아라비아 리아드) 연례총회에 참석하여 디지털헬스 글로벌 중심국가로 도약하기 위한 의료기기 분야 국제 협력 네트워크를 강화하고 국산 제품의 수출지원 방안을 모색했다. * GHWP(Global Harmonization Working Party) : 의료기기 국제 규제 조화를 위해 1996년 발족한 협력기구. 현재 미국, 일본, 중국, 싱가포르 등 세계 33개 회원국에서 참여 중이며, 기술위원회(Technical Committee)와 9개의 실무그룹(Working Group)으로 구성. 우리나라는 ’15~’17년 의장국 수행 이번 총회에서 식약처는 우수한 허가·심사 규제역량을 인정받아 ‘의료기기 허가 실무그룹(실무그룹1)’ 의장직을 연임(3년 임기)하게 되었다. 아울러 식약처는 IMDRF* 의장국으로 활동하면서 식약처의 인공지능 의료기기 가이드라인을 국제 공통 가이드라인으로 채택시킨 경험과 전문성을 바탕으로, GHWP에서 식약처의 ‘인공지능 기반 조직병리 체외진단 의료기기(소프트웨어) 허가심사 가이드라인’을 국제 공통 가이드라인으로 채택하기 위한 논의를 시작했다. * 국제의료기기규제당국자포럼(International Medical Device Regulatory Forum, IMDRF) : 의료기기 사전·사후 전주기에 대한 국제 규제 조화·단일화를 촉진하기 위해 구성된 미국 유럽 등 11개국 규제당국자 간 협의체. 우리나라는 ’21년 의장국으로 활동 또한 이번 총회에서는 GHWP 회원국이 의료기기의 허가사항을 변경할 때 적용하는 가이드라인*에 식약처의 ‘인공지능 의료기기 허가심사 가이드라인’이 중요한 참고 가이드라인으로 추가되었다. * Categorization of Changes to a Registered Medical Device 참고로 이번 GHWP 연례총회에서 ‘디지털헬스기기의 적용 확대’를 특별 주제로 선정해 논의했으며, 우리나라는 식약처, 산업계, 병원 등에서 연자로 참석하여 국내 선진 규제 시스템과 혁신제품 활용사례를 발표했다. 특히 선제적 가이드라인 마련 등 맞춤형 규제지원을 받아 국내 최초로 허가된 디지털치료기기*, 디지털 기술이 적용된 스마트병원, 다양한 인공지능 의료기기 활용사례 등이 많은 관심을 받았다. * 불면증 인지행동 치료용 디지털치료기기(’23.2.15. 허가) 식약처는 앞으로 규제과학 전문성을 기반으로 GPS* 전략을 적극 추진하여 의료기기 분야 국제 규제 조화를 선도하고 우수한 국산 의료기기의 해외시장 진출을 지원하겠다고 밝혔다. * G(글로벌 리더로 도약), P(국제 파트너쉽 확대), S(수출지원 서포터) -
![[미국] 미국 특허심판원의 판례분석 - 청구 해석의 기준 제시](http://www.stdnews.kr/data/file/news/thumb/thumb-988342002_XUfNAGaI_8985a89d8fda06d24f05a7a4b846c53ebd70eeb3_200x180.jpg) [미국] 미국 특허심판원의 판례분석 - 청구 해석의 기준 제시미국 특허심판원은 IPR(Inter partes Review), PGR(Post-Grant Review), CBM(Covered Business Method)중에 적용되는 클레임 구성 표준을 변경하는 최종 규칙을 발표했다.최종 규칙은 2012년 9월 16일부터 온라인으로 제공된 이후 미국특허청이 클레임을 해석하는데 사용했던 가장 광범위하고 합리적인 해석 표준을 필립스 표준으로 대체한다.필립스 표준은 특허 침해소송에서 특허 청구를 해석하는데 사용되는 것과 동일한 청구 구성 표준이다. 즉 특허심판원 청구 해석의 기준을 소송시의 청구 해석 기준과 동일하다고 판단한다. 판결의 세부 내용은 아래와 같다.Final Rule Changing Claim ConstructionMoving away from “Broadest Reasonable Interpretation”Moving to Phillips Standard:•The new standard applies to inter partes review, post grant review and the covered business method proceedings before the PTAB.•Phillips Standard: claims be given their ordinary and customary meaning.•PTAB will take into consideration any prior claim construction determination that has been made in a civil action or from ITC, if that prior claim construction is timely made of record.•USPTO is hoping to achieve greater consistency and harmonization with the federal courts and the ITC.•This rule will not be retroactively applied and will apply to IPR, PGR and CBM cases filed on or after the Nov. 13, 2018.Potential Effects of Change in Standard:•This will likely result in less claim cancellation during IPR proceedings, since claims will be given narrower interpretation.•In the long run, this may create more patent litigations as the patent owner’s right increase.•USPTO is trying to give more definiteness and clarity to patent owners in enforcing their patents.•Since there is a trend in increase of patent owner’s rights, it is very important to secure patents to protect/enforce IP rights. Current Status of Proceedings at PTAB:
[미국] 미국 특허심판원의 판례분석 - 청구 해석의 기준 제시미국 특허심판원은 IPR(Inter partes Review), PGR(Post-Grant Review), CBM(Covered Business Method)중에 적용되는 클레임 구성 표준을 변경하는 최종 규칙을 발표했다.최종 규칙은 2012년 9월 16일부터 온라인으로 제공된 이후 미국특허청이 클레임을 해석하는데 사용했던 가장 광범위하고 합리적인 해석 표준을 필립스 표준으로 대체한다.필립스 표준은 특허 침해소송에서 특허 청구를 해석하는데 사용되는 것과 동일한 청구 구성 표준이다. 즉 특허심판원 청구 해석의 기준을 소송시의 청구 해석 기준과 동일하다고 판단한다. 판결의 세부 내용은 아래와 같다.Final Rule Changing Claim ConstructionMoving away from “Broadest Reasonable Interpretation”Moving to Phillips Standard:•The new standard applies to inter partes review, post grant review and the covered business method proceedings before the PTAB.•Phillips Standard: claims be given their ordinary and customary meaning.•PTAB will take into consideration any prior claim construction determination that has been made in a civil action or from ITC, if that prior claim construction is timely made of record.•USPTO is hoping to achieve greater consistency and harmonization with the federal courts and the ITC.•This rule will not be retroactively applied and will apply to IPR, PGR and CBM cases filed on or after the Nov. 13, 2018.Potential Effects of Change in Standard:•This will likely result in less claim cancellation during IPR proceedings, since claims will be given narrower interpretation.•In the long run, this may create more patent litigations as the patent owner’s right increase.•USPTO is trying to give more definiteness and clarity to patent owners in enforcing their patents.•Since there is a trend in increase of patent owner’s rights, it is very important to secure patents to protect/enforce IP rights. Current Status of Proceedings at PTAB: -
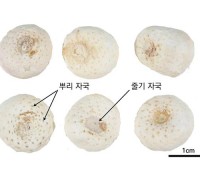 식약처, 생약 품질관리 국제기준 선도식품의약품안전처(처장 오유경, 이하 식약처)는 생약 품질관리에 대한 최신 규제정보를 공유하고 국제조화를 도모하기 위한 ‘생약규격국제조화포럼’(이하 FHH) 제2분과(품질보증) 연례회의를 9월 30일 온라인으로 개최한다고 밝혔다. 생약규격국제조화포럼(FHH, Forum for the Harmonization of Herbal medicines)는 2001년에 구성된 서태평양지역 전통 의약품 사용 6개국(한국·중국·일본·베트남·싱가포르·홍콩) 규제당국의 협의체로, 상임위원회와 ▲공정서 ▲품질보증 ▲부작용 등 총 3개 분과로 운영된다. 식약처는 제2분과인 품질보증을 주관하고 있다. 이번 회의에서는 ▲식품의약품안전평가원(이하 평가원)에서 개발한 한약재 ‘반하’의 시험법에 대한 표준도감(안) 확정 ▲한국·홍콩의 위변조 한약재 감별법 ▲천연물의약품의 품질평가에 대한 국제조화 방안에 대해 논의한다고 밝혔다. 표준도감이란 한약(생약) 품질관리에 참고하기 위해 기원종이 확인된 한약(생약)에 대한 이화학·유전자 분석 시험법 및 분석결과(크로마토그램 등)를 담은 도감이다. ▲반하 / 사진제공 : 식품의약품안전처 반하란 반하의 덩이줄기로서 주피를 완전히 제거한 것으로 주요 효능으로는 비위(소화기관)에 작용하여 담을 없애고 구토나 소화불량을 다스린다. 평가원은 매년 제2분과 연례 국제회의를 개최하고 있으며, 이번 회의는 회원국 규제당국자 외에 세계보건기구 서태평양지역사무처(WHO/WPRO), 미국, 스위스 전문가 등 총 34명이 참석한다. 첫 번째 세션에서는 평가원에서 개발한 한약재 ‘반하’의 이화학·유전자분석 시험법에 대해 홍콩, 일본, 베트남에서 참여한 교차검증 결과를 심도 있게 검토하고, 한국의 ‘한약재 관능검사 해설서’와 홍콩의 ‘오ㆍ혼용 중약재 감별집’을 이용하여 한약재의 정확한 기원종 감별을 위한 국제협력 방안을 논의한다. 식약처는 이번 회의에서 ‘반하’ 표준도감(안)을 확정하고, 내년 제20차 FHH 상임위원회(홍콩)에서 표준도감으로 채택을 추진할 예정이라고 밝혔다. 표준도감으로 채택되면 FHH 각국에서 한약재 품질관리 참고자료로 활용되어 기원이 명확한 ‘반하’가 수출입 될 것으로 기대합니다. 두 번째 세션에서는 ‘천연물의약품 품질평가의 미래와 국제조화’를주제로 평가원과 홍콩 위생성(DH, Department of Health)이 각각 한국과 홍콩의 천연물의약품 품질심사기술을 소개한다. 이어서 한국과학기술연구원(KIST) 천연물연구소에서도 ‘천연물의약품의 품질평가를 위한 인공지능기술의 미래 역할’에 대해 발표한다. 식약처는 이번 국제회의가 첨단기술을 활용한 생약 품질관리 기술 개발을 촉진하고 생약 품질관리 분야의 국제조화에 기여할 것으로 기대하며 앞으로도 적극적으로 국제협력을 추진하여 생약 품질관리 선도국으로 위상을 높이겠다고 밝혔다.
식약처, 생약 품질관리 국제기준 선도식품의약품안전처(처장 오유경, 이하 식약처)는 생약 품질관리에 대한 최신 규제정보를 공유하고 국제조화를 도모하기 위한 ‘생약규격국제조화포럼’(이하 FHH) 제2분과(품질보증) 연례회의를 9월 30일 온라인으로 개최한다고 밝혔다. 생약규격국제조화포럼(FHH, Forum for the Harmonization of Herbal medicines)는 2001년에 구성된 서태평양지역 전통 의약품 사용 6개국(한국·중국·일본·베트남·싱가포르·홍콩) 규제당국의 협의체로, 상임위원회와 ▲공정서 ▲품질보증 ▲부작용 등 총 3개 분과로 운영된다. 식약처는 제2분과인 품질보증을 주관하고 있다. 이번 회의에서는 ▲식품의약품안전평가원(이하 평가원)에서 개발한 한약재 ‘반하’의 시험법에 대한 표준도감(안) 확정 ▲한국·홍콩의 위변조 한약재 감별법 ▲천연물의약품의 품질평가에 대한 국제조화 방안에 대해 논의한다고 밝혔다. 표준도감이란 한약(생약) 품질관리에 참고하기 위해 기원종이 확인된 한약(생약)에 대한 이화학·유전자 분석 시험법 및 분석결과(크로마토그램 등)를 담은 도감이다. ▲반하 / 사진제공 : 식품의약품안전처 반하란 반하의 덩이줄기로서 주피를 완전히 제거한 것으로 주요 효능으로는 비위(소화기관)에 작용하여 담을 없애고 구토나 소화불량을 다스린다. 평가원은 매년 제2분과 연례 국제회의를 개최하고 있으며, 이번 회의는 회원국 규제당국자 외에 세계보건기구 서태평양지역사무처(WHO/WPRO), 미국, 스위스 전문가 등 총 34명이 참석한다. 첫 번째 세션에서는 평가원에서 개발한 한약재 ‘반하’의 이화학·유전자분석 시험법에 대해 홍콩, 일본, 베트남에서 참여한 교차검증 결과를 심도 있게 검토하고, 한국의 ‘한약재 관능검사 해설서’와 홍콩의 ‘오ㆍ혼용 중약재 감별집’을 이용하여 한약재의 정확한 기원종 감별을 위한 국제협력 방안을 논의한다. 식약처는 이번 회의에서 ‘반하’ 표준도감(안)을 확정하고, 내년 제20차 FHH 상임위원회(홍콩)에서 표준도감으로 채택을 추진할 예정이라고 밝혔다. 표준도감으로 채택되면 FHH 각국에서 한약재 품질관리 참고자료로 활용되어 기원이 명확한 ‘반하’가 수출입 될 것으로 기대합니다. 두 번째 세션에서는 ‘천연물의약품 품질평가의 미래와 국제조화’를주제로 평가원과 홍콩 위생성(DH, Department of Health)이 각각 한국과 홍콩의 천연물의약품 품질심사기술을 소개한다. 이어서 한국과학기술연구원(KIST) 천연물연구소에서도 ‘천연물의약품의 품질평가를 위한 인공지능기술의 미래 역할’에 대해 발표한다. 식약처는 이번 국제회의가 첨단기술을 활용한 생약 품질관리 기술 개발을 촉진하고 생약 품질관리 분야의 국제조화에 기여할 것으로 기대하며 앞으로도 적극적으로 국제협력을 추진하여 생약 품질관리 선도국으로 위상을 높이겠다고 밝혔다.


![[특집-ISO/IEC JTC 1/SC 17 활동] 35. Result of voting on SR Ballot for ISO/](http://www.stdnews.kr/data/file/news/thumb/thumb-3555379571_4cufp2BH_756bcefa64e6169e58646ad7b061ecbec455fb11_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 34. Result of voting on SR ballot for ISO/](http://www.stdnews.kr/data/file/news/thumb/thumb-3555380113_kIQxAlfN_727cc6e35ccb9d5e6c07574a3b3a2ab9db104d48_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 33. Result of voting on SR ballot for ISO/](http://www.stdnews.kr/data/file/news/thumb/thumb-32068165_R52GPIij_2bca2660198a937d2534db7bfd9fc8174a76cfa2_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 32. Result of voting on SR Ballot for ISO/](http://www.stdnews.kr/data/file/news/thumb/thumb-32068165_TxRrtYEa_c36d1a53acc15db7e18fae132ffef64e11bda43c_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 31. Result of voting on SR Ballot for ISO/](http://www.stdnews.kr/data/file/news/thumb/thumb-3555377690_nrjmWhSf_d9b63299e7f3f52053141cae28f32f7df40b5918_340x240.jpg)


![[일본] 요코하마(横浜), 3월 원격근무로 일하는 50대 여성이 장시간 노동을 강요받아 적응장애가 발병해 산재로 인정받아](http://www.stdnews.kr/data/file/news/thumb/thumb-3555377672_BapV2SmF_41a011a26290be1daa3f6a5220df7b8b6d167f69_340x240.jpg)
![[인도] 마하라슈트라주 식품의약국(Maharashtra FDA), 맥도날드 상품명에 치즈를 잘못 표기해 소비자 기만 지적](http://www.stdnews.kr/data/file/news/thumb/thumb-3743818281_Uu5GpcKZ_6890f33f4b087f58686ed20e46a04bbb79ad883e_340x240.jpg)
![[남아공] 토코만 푸드(Thokoman Foods), 자사 땅콩버터 식품 안전성 재확인](http://www.stdnews.kr/data/file/news/thumb/thumb-3743818281_h5HrK0kT_c2453abdb4577a16b34590f5b8f76de9c2a95469_340x240.jpg)
![[일본] 혼다(ホンダ), 2030년까지 전기자동차(EV)를 중심으로 하는 전동화와 소트프웨어 개발에 10조 엔을 투자할 계획](http://www.stdnews.kr/data/file/news/thumb/thumb-3555381172_1g5z7YDN_4db7699b271b5e9dbbe1a4f6dc69fb01a9881abb_340x240.jpg)
![[일본] 자민당(自民党), 기업이 직원을 고객의 '카스하라(カスハラ)로부터 보호를 의무로 하는 방안을 고려 중](http://www.stdnews.kr/data/file/news/thumb/thumb-3555381172_PCNyaL1v_9f9b79d526b4be07024401e874fe26f618a42e7c_340x240.jpg)
![[일본] 총무성(総務省), 2023년 기준 전국의 빈집은 900만 호로 사상 최고치 기록](http://www.stdnews.kr/data/file/news/thumb/thumb-3555379571_qr01mWC9_fef7fa874e596585a04ee2dae235376595341779_340x240.jpg)
![[특집-기상기후재난] 한국중부발전(주) 신정철 선임 인터뷰 - 행정안전부 뿐 아니라 기상기후 연계조직 모두가 참여하는 협의체가](http://www.stdnews.kr/data/file/news/thumb/thumb-3555374516_iKWwUBas_9c1729f1e3977ee50c398986e7f98d5002a57deb_340x240.jpg)
![[특집-기상기후재난] (주)비밍코어 정성민 대표 인터뷰 - 인공지능(AI) 활용한 기후재난 대처 솔루션 개발](http://www.stdnews.kr/data/file/news/thumb/thumb-3555374391_0JZYhIcj_dca23c54fc7923952082a9d7af92db00b9dd33c9_340x240.jpg)
![[기획-표준 전문가] 한국투자증권 김범수 FC 인터뷰 - 표준전문가 양성 교육이 지속되길 희망](http://www.stdnews.kr/data/file/news/thumb/thumb-3555374114_Np9hM7aC_e6ffa916aade15e1c301badf3132ed3f0551a900_340x240.jpg)
![[특집-기상기후재난] 행정안전부 안전교육 전문인력 유정희 강사 인터뷰 - 기상기후재난예방 전문가 양성 시급](http://www.stdnews.kr/data/file/news/thumb/thumb-3555374240_gOmdLG10_cfc17ed887dccc93f503013bf794ed568a5d40dc_340x240.jpg)
![[특집-기상기후재난] (주)이토스 김형식 대표 인터뷰 - 재난을 사전에 예측·예방할 기술개발 시급](http://www.stdnews.kr/data/file/news/thumb/thumb-32068165_lmUrCBIn_797dc8926bb7d90542546463cc73e6233f0bbb46_340x240.png)